Activité « CONFIGURATION ÉLECTRONIQUE D’UN ATOME »
LIEN AVEC LE TABLEAU PÉRIODIQUE
1. CONFIGURATION ÉLECTRONIQUE D’UN ATOME
1.1. Cortége électronique
- Un atome possède un ensemble d’électrons appelé cortège électronique.
- Un atome étant électriquement neutre : le nombre d’électrons est égal au nombre de protons (dans son noyau).
- Le cortège électronique d’un atome est donc constitué de Z électrons.
1.2. Configuration électronique
- Dans la frise suivante, on peut zoomer sur le modèle de Bohr

Figure 1 : Modèles successifs de l’atome dans l’histoire des sciences
- Dans son modèle, Bohr distingue, organise les électrons en couches électroniques.
- Plus bas, une vidéo (toujours aussi claire et concise) de Florence Raffin sur le sujet :
- Pour Z \(\leq\) 18
- 3 couches 1,2 et 3.
- 2 sous couches :
- s (avec, au maximum, 2 électrons)
- p (avec, au maximum, 6 électrons)

- Pour obtenir la configuration d’un atome, on remplit dans l’ordre : 1s \(\Rightarrow\) 2s \(\Rightarrow\) 2p \(\Rightarrow\) 3s \(\Rightarrow\) 2p
- La couche externe est la dernière couche remplie. Les électrons concernés par cette couche externe sont les électrons de valence.
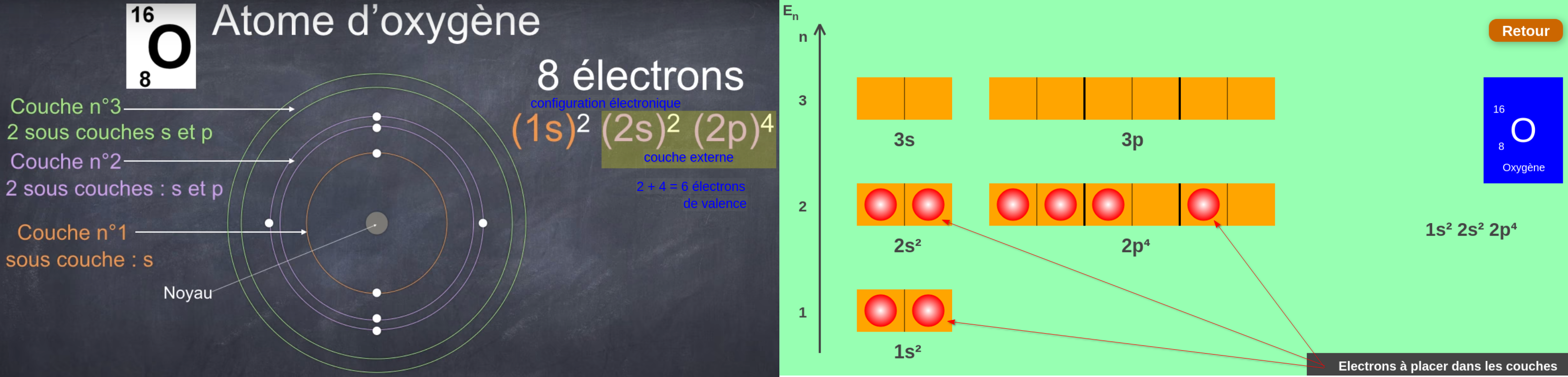
Figure 2 : Exemple de la configuration électronique de l’atome d’oxygène \((1s)^{2}(2s)^{2}(2p)^{4}\)
- Autres exemples :
- Configuration électronique de l’atome He à l’état fondamental : \((1s)^{2}\)
- Configuration électronique de l’atome Be à l’état fondamental : \((1s)^{2}(2s)^{2}\)
- Configuration électronique de l’atome P à l’état fondamental : \((1s)^{2}(2s)^{2}(2p)^{6}(3s)^{2}(3p)^{3}\)
- Retrouver la configuration électroniques de l’oxygène O en utilisant l’animation sur Labosims (Auteur : Samuel JACQUINET)
- Retrouver la configuration électronique du phosphore en utilisant l’animation sur Labosims (Auteur : Samuel JACQUINET)
- Autres exemples dans le tableau périodique « simplifié » :

- Dans le tableau précédent, légender la première case
- en désignant Z (numéro atomique)
- en désignant la configuration électronique
- Compléter le tableau périodique simplifié en ajoutant les configurations électroniques (à l’état fondamental) manquantes (atomes H, Li, C, Ne, Na, Si, Ar)
- Choisir 3 atomes au hasard (avec \(3 \le Z \le 18\)) et additionner les nombres d’électrons s et p. Pour chaque cas, comparer au numéro atomique Z.
- Comparer la valeur de n des derniers électrons d’un atome au numéro de la ligne dans laquelle il se trouve.
2. ÉLECTRONS DE VALENCE
- La couche externe est la dernière couche remplie.
- Les électrons concernés par cette couche externe sont les électrons de valence.
- Les électrons de valence d’un atome (de numéro atomique \(Z \le 18\)) sont donc les électrons ns et np (avec n = 1, 2 ou 3), où n a la plus grande valeur dans la configuration électronique de l’atome.
- Déterminer le nombre d’électrons de valence pour chacun des atomes suivants H, Li, C, Ne, Na, Si, Ar. (On pourra se contenter de les noter dans chacune des cases du tableau en légendant dans la première case)
- Pour les atomes des éléments d’une même colonne déterminer un point commun à leur nombre d’électrons de valence.
- Comparer le nombre d’électrons de valence d’un atome au chiffre des unités du numéro de colonne à laquelle il appartient.
Pour vérifier les configurations électroniques des atomes vues précédemment, on peut se connecter sur le site www.ptable.com (onglet « Electrons ») (Choisir l’icône « Top bar »)

3. FAMILLES CHIMIQUES
Les élements chimiques qui ont des propriétés chimiques communes constituent une famille chimique.
4.
- Dans le tableau Ptable sur le site www.ptable.com (onglet
« Propriétés »). Repérer les éléments appartenant aux
familles suivantes :
- alcalins (ou « alcali » sur Ptable) : cases à colorier sur le tableau initial.
- halogènes : (Non-métal, plus précisément colonne 17) avec une autre couleur.
- gaz nobles : idem avec une autre couleur.
Dans le tableau périodique, comment sont regroupés les éléments d’une même famille ?
- Pour les éléments d’une même famille, comparer le nombre d’électron de valence.

5. LA FAMILLE DES GAZ NOBLES
- Dans le tableau périodique, indiquer où se trouvent les éléments de la famille des gaz nobles. Quel est le nombre d’électrons de valence que possèdent les atomes de gaz nobles autres que l’hélium.
- Un atome de numéro atomique \(Z \le 18\) peut-il avoir plus d’électrons de valence que les atomes de gaz nobles autre que l’hélium.
- Dans le tableau Ptable sur le site www.ptable.com (onglet « Composés »),

- « Drag elements inside to create compounds »

- « Drag elements inside to create compounds » ici « O »
Pour les trois premiers éléments des gaz nobles, vérifier le peu d’associations possibles de ces atomes « nobles » avec d’autres atomes. Moins un atome s’engage dans des associations, plus on dit qu’il est « stable »
- Établir un lien entre
- la stabilité des gaz nobles
- et le nombre d’électrons de valence de leurs atomes.
